Dia-Präsentation von Solvay Pharma aus dem Jahr 2003 Eprosartan (65 Abbildungen) Übersicht Gesamtpräsentation zum Download (rechte Maustaste und "Ziel speichern unter..." klicken)
| ||||||||||||||||
Abbildung 2: Pharmakologie der AT1-Blocker (2/2) Im Vergleich zu anderen AT1-Blockern besitzt Eprosartan eine kurze Halbwertszeit und ein geringes Distributionsvolumen. Es wird im Gegensatz zu Losartan, Irbesartan, Olmesartan und Candesartan nicht durch das Cytochrom P450-System der Leber verstoffwechselt, eine häufige Ursache medikamentöser Wechselwirkungen. Eprosartan weist einen gerade für Patienten mit renalen Erkrankungen vorteilhaftes Exkretionsprofil auf. Die Angeben der Tabelle beziehen sich auf die Exkretion nach intravenöser Injektion; nach oraler Gabe werden 90 % des Wirkstoffes mit dem Fäzes und nur 7 % mit dem Urin ausgeschieden. Wong PC, Christ DD, Wong YN et al.: Nonpeptide angiotensin II receptor antagonist: pharmacokinetics and pharmacodynamics in rats of EXP3174, an active metabolite of losartan. Pharmacology 1996; 52 (1): 25–9 Brunner HR: The new angiotensin II receptor antagonist, irbesartan: pharmacokinetic and pharmacodynamic considerations. Am J Hypertens 1997; 10 (12 Pt 2): 311S–317S Buter H, Navis GY, Woittez AJ et al.: Pharmacokinetics and pharmacodynamics of candesartan cilexitil in patients with normal to severely impaired renal function. Eur J Clin Pharmacol 1999; 54 (12): 953–8 Kovacs SJ, Tenero DM, Martin DE et al.: Pharmacokinetics and protein binding of eprosartan in hemodialysis-dependent patients with end-stage renal disease. Pharmacotherapy 1999; 19 (5): 612–9 |
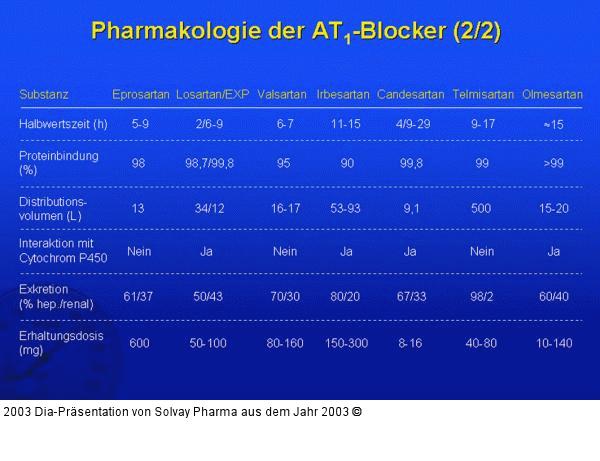
Abbildung 2: Pharmakologie der AT1-Blocker (2/2)
Im Vergleich zu anderen AT1-Blockern besitzt Eprosartan eine kurze Halbwertszeit und ein geringes Distributionsvolumen. Es wird im Gegensatz zu Losartan, Irbesartan, Olmesartan und Candesartan nicht durch das Cytochrom P450-System der Leber verstoffwechselt, eine häufige Ursache medikamentöser Wechselwirkungen. Eprosartan weist einen gerade für Patienten mit renalen Erkrankungen vorteilhaftes Exkretionsprofil auf. Die Angeben der Tabelle beziehen sich auf die Exkretion nach intravenöser Injektion; nach oraler Gabe werden 90 % des Wirkstoffes mit dem Fäzes und nur 7 % mit dem Urin ausgeschieden. Wong PC, Christ DD, Wong YN et al.: Nonpeptide angiotensin II receptor antagonist: pharmacokinetics and pharmacodynamics in rats of EXP3174, an active metabolite of losartan. Pharmacology 1996; 52 (1): 25–9 Brunner HR: The new angiotensin II receptor antagonist, irbesartan: pharmacokinetic and pharmacodynamic considerations. Am J Hypertens 1997; 10 (12 Pt 2): 311S–317S Buter H, Navis GY, Woittez AJ et al.: Pharmacokinetics and pharmacodynamics of candesartan cilexitil in patients with normal to severely impaired renal function. Eur J Clin Pharmacol 1999; 54 (12): 953–8 Kovacs SJ, Tenero DM, Martin DE et al.: Pharmacokinetics and protein binding of eprosartan in hemodialysis-dependent patients with end-stage renal disease. Pharmacotherapy 1999; 19 (5): 612–9 |







